Utilización de ventilación no invasiva inicial en una Unidad de
Cuidados Intensivos Pediátricos
[Use of initial non-invasive ventilation in a Pediatric Intensive Care
Unit]
Doris Musa,* María Mercedes
Ortuondo, Lara Quiroz, Micaela Vallejos
Equipo de Kinesiología Pediátrica, Sanatorio Mater Dei, Ciudad
Autónoma de Buenos Aires, Argentina
* Correspondencia: doris.musa@smdei.com
Las autoras no
declaran conflictos de intereses.
https://doi.org/10.64955/jratiy2025x923
Resumen
La ventilación no invasiva inicial (VNIi) es una alternativa para
evitar la intubación y la ventilación mecánica invasiva (VMI) en el tratamiento
de la insuficiencia respiratoria aguda de lactantes y niños; disminuye la
morbimortalidad y los días de internación. Objetivo: Conocer la tasa de éxito de la VNIi en
pacientes de una unidad de cuidados intensivos pediátricos (UCIP) y explorar
los factores asociados al éxito. Diseño: Descriptivo, observacional y retrospectivo. Pacientes y métodos: Se recolectó
información de la base de datos del equipo de kinesiología pediátrica sobre los
pacientes que ingresaron en VNIi entre 2021 y 2023, y se corroboró con las
historias clínicas digitales de cada paciente. Se registraron: edad, sexo,
índice de mortalidad pediátrica 3, diagnóstico, comorbilidades, días de VNIi,
índice de inicio de SpO2/FiO2 (SaFiO2), causas del fracaso de la VNIi y días de internación. Se consideró
que la VNIi era exitosa si no era necesaria la intubación. Resultados: De los 780 pacientes ingresados en la
UCIP entre enero de 2021 y agosto 2023, 159 requirieron VNIi. La tasa de éxito
fue del 71,1%. La SaFiO2 inicial tuvo una asociación estadísticamente significativa e
independiente con el éxito de la VNIi. El grupo con VNIi exitosa permaneció
internado durante 7 días (RIC 6-9), mientras que el grupo de VNIi fallida lo
hizo durante 14.5 días (RIC 11-21) (p <0,001). Conclusiones: La VNIi exitosa evitó el ingreso de un
alto porcentaje de pacientes a la intubación y la VMI. La SaFiO2 inicial es una variable significativa e independiente del éxito de la
VNIi.
Palabras clave: Unidad de cuidados intensivos
pediátricos; insuficiencia respiratoria aguda; ventilación no invasiva
electiva; presión positiva binivel.
Abstract
Initial non-invasive ventilation (iNIV) is an alternative to avoid
intubation and invasive mechanical ventilation (IMV) in the treatment of acute
respiratory failure in infants and children; reduces morbidity and mortality
and days of hospitalization. Objective: To know the
success rate of iNIV in patients in a pediatric intensive care unit (PICU) and
explore the factors associated with success. Design: Descriptive, observational and
retrospective. Patients and methods: Information was collected from the pediatric kinesiology team’s database
on patients admitted to iNIV between 2021 and 2023, and corroborated with the
digital medical records of each patient. The following were recorded: age, sex,
pediatric mortality index 3, diagnosis, comorbidities, days of iNIV, SpO2/FiO2
onset index (SaFiO2), causes of iNIV failure, and days of hospitalization. iNIV
was considered successful if intubation was not necessary. Results: Of the 780 patients admitted to the PICU
between January 2021 and August 2023, 159 required iNIV. The success rate was
71.1%. Baseline SaFiO2 had a statistically significant and independent
association with iNIV success. The group with successful iNIV remained
hospitalized for 7 days (IQR 6-9), while the group with failed iNIV remained
hospitalized for 14.5 days (IQR 11-21) (p <0.001). Conclusions: Successful iNIV prevented a high
percentage of patients from being admitted for intubation and IMV. Initial
SaFiO2 is a significant and independent variable of iNIV success.
Keywords: Pediatric intensive care unit; acute
respiratory failure; initial non-invasive ventilation; bilevel positive airway
pressure.
Introducción
En el mundo,
ocurren entre 120 y 156 millones de casos de infecciones respiratorias agudas
(IRA) por año, que ocasionan 1,4 millones de muertes en pacientes <5 años de
edad. Más del 95% de estas muertes se producen en países de ingresos bajos y
medios.1
La
insuficiencia respiratoria aguda se produce cuando existe un desequilibrio
pulmonar entre el ingreso de oxígeno y la eliminación del dióxido de carbono
que impide satisfacer las demandas metabólicas.2 Dentro de las IRA se encuentran las
infecciones respiratorias agudas bajas las cuales representan una importante
causa de morbimortalidad en pediatría.1 En diferentes estudios, se demostró
que es uno de los principales motivos de consulta en los servicios de atención
de la salud; el 25% de los pacientes necesita internación3 y, de ellos, entre el 30% y el 50% requiere de
terapia intensiva pediátrica y algún tipo de soporte ventilatorio mecánico.4
Actualmente,
la evidencia sostiene que la ventilación no invasiva inicial (VNIi) en la
población pediátrica se puede implementar como primera opción de soporte
ventilatorio y, de ese modo, evitar la ventilación mecánica invasiva (VMI) la
cual requiere de intubación.5-6 En
comparación con la VMI, la VNIi tiene ventajas, tales como menor riesgo de
neumonía asociada con la ventilación mecánica, de lesión de las vías
respiratorias superiores, de disfunción de las cuerdas vocales posextubación,
menor necesidad de sedoanalgesia, lo que resulta en un menor riesgo de
debilidad muscular adquirida, morbimortalidad y de días de internación.7-12
En nuestra
Unidad de Cuidados Intensivos Pediátricos (UCIP), la VNIi es un soporte
utilizado con frecuencia. Aún no contamos con datos sobre los resultados de la
implementación en nuestra Unidad; por lo tanto, el objetivo de este estudio
fue conocer la tasa de éxito de la VNIi en pacientes internados en una UCIP y
explorar los factores asociados al éxito.
Materiales y Métodos
Se llevó a
cabo un estudio descriptivo, observacional y retrospectivo. Los datos se
recolectaron mediante la revisión de la base de datos del equipo de
kinesiología pediátrica que, luego, fueron corroborados con las historias
clínicas digitales de cada paciente.
Se incluyó
pacientes de 1 mes a 16 años de edad, internados en la UCIP del Sanatorio Mater
Dei de la Ciudad Autónoma de Buenos Aires, entre enero de 2021 y agosto de
2023, que ingresaron desde el sector de guardia o del piso de internación con
requerimiento de VNIi durante la IRA y no mejoraron luego de implementar la
oxigenoterapia convencional o de alto flujo, junto con el tratamiento médico
indicado. Quedaron excluidos aquellos pacientes que recibían ventilación no
invasiva domiciliaria antes de la internación, con esfuerzo terapéutico
adecuado, derivados de la Unidad de Cuidados Intensivos Neonatales o derivados
a otra institución.
Descripción de la VNIi
Antes de
iniciar la VNIi, se colocó una película barrera no irritante (3M™ Cavilon) y
por encima cinta quirúrgica (3M™ Medipore-H™) en las zonas de apoyo de la
interfase para proteger la piel de los pacientes. Los respiradores utilizados
fueron Puritan Bennett™ 840 (Covidien LLC, MA, EE.UU.), Neumovent TS (Tecme SA,
Argentina) y Neumovent Advance (Tecme SA, Argentina). Las interfases utilizadas
fueron: nasales: Respireo™ Soft Baby & Child; oronasales: Respironics
AF531, modelos S, M, L (Philips); total face: Respironics PerforMax Total Face,
modelos XXS, XS, S, L, XL (Philips). Siempre se utilizó un sistema de humidificación
activa Fisher & Paykel™ MR 410 y MR 810. Los sujetadores de dichas
interfases fueron arneses Philips para PerforMax y, para las interfases
oronasales, el arnés 4 Pos.Clip P Af531 Respironics.
En relación
con la titulación de inicio de la VNIi, se utilizó la modalidad binivelada,
asistocontrolada, considerando una presión positiva al final de la espiración
(PEEP) basal de 5 cmH2O, que se fue modificando junto con la
fracción inspirada de oxígeno (FiO2) para obtener una saturación de
oxígeno >92%. Se utilizó una presión positiva inspiratoria necesaria para
lograr un volumen espirado de 8 a 10 ml/kg, también se valoró la mecánica
ventilatoria del paciente. Si era necesario, se administraba sedación para una
mejor adaptación.
Al iniciar la
VNIi y a las dos horas de la implementación, se determinaron los siguientes
parámetros: frecuencia cardíaca, frecuencia respiratoria, saturación de
oxígeno, mecánica ventilatoria (evaluando la presencia de tiraje intercostal o
subcostal o supraesternal o generalizado, uso de músculos accesorios o
respiración en balancín) y se utilizaron las escalas de gravedad de Tal
modificada y de Wood-Downes modificada por Ferrés, según necesidad.13,14 Desde el monitoreo ventilatorio, se
observó: la PEEP, la presión positiva inspiratoria, la FiO2 y la
modalidad ventilatoria requerida.
Cuando los
parámetros clínicos iniciales mejoraron, se disminuyeron progresivamente la FiO2 y las
presiones, y también se probaron períodos de tolerancia sin presión positiva,
hasta alcanzar el destete completo de la VNIi.
Variables de estudio
Como
variables o resultados primarios se consideró el éxito o fracaso de la VNIi, se
definió como éxito al destete de la VNI sin necesidad de intubación y fracaso
como la necesidad de intubación. Asimismo, se registraron las siguientes
variables: sexo, edad (meses), índice de mortalidad pediátrica 3, diagnóstico
al ingreso, comorbilidades, SaFiO2, días totales de VNIi, días totales de
internación, requerimiento de sedación durante la VNIi, causa de fracaso de la
VNIi, rescate microbiológico a través de muestra de secreciones y mortalidad.
Análisis estadístico
Las variables
categóricas se expresan como número de presentación y porcentaje.
Las variables
continuas que asumieron una distribución normal se muestran como media y
desviación estándar, de lo contrario se utilizaron la mediana y el rango
intercuartílico (RIC). Para determinar la distribución de la muestra de las
variables continuas se utilizaron pruebas estadísticas (Shapiro-Wilk) y métodos
gráficos (histogramas y cuantil-cuantil).
Para comparar
las variables categóricas se utilizó la prueba χ2 o la prueba exacta de Fisher, según
correspondiera. Las variables continuas se compararon con la prueba de la t de
Student para muestras independientes o la prueba de Mann-Whitney, según
correspondiera.
Se realizó un
análisis de regresión logística para explorar las variables asociadas con el
éxito de la VNIi. Para determinar el modelo que mejor se ajustó a los datos
observados se consideraron aquellas variables con un valor p <0,10 en el
análisis univariado. Se utilizó el criterio de información de Akaike con el
método de selección paso a paso (stepwise selection).15 Se priorizó identificar el modelo más
parsimonioso, con mejor ajuste y con asociación epidemiológica en la mayoría de
sus variables explicativas.
La capacidad
del modelo para discriminar aquellos factores asociados al éxito en la
implementación de VNIi se evaluó utilizando el área bajo la curva (area
under the receiver operating characteristics curve, AUC). El AUC presenta
un rango de 0 a 1; un AUC <0,5 indica que el desempeño del modelo es peor
que el azar, mientras que un AUC = 1 indica un desempeño perfecto. Las AUC
>0,7 y >0,9 se consideran desempeños aceptables y excelentes,
respectivamente.16
Como medida
de asociación se reportaron los cocientes de posibilidades (odds ratios,
OR) con sus respectivos intervalos de confianza del 95% (IC95%). Aquellos casos
con datos perdidos en las variables de interés fueron excluidos de este
análisis. Se consideró significativo un valor p <0,05.
Los datos se
analizaron con el programa IBM SPSS Macintosh, versión 24.0 (IBM Corp., Armonk,
NY, EE.UU.).
Resultados
Características de la muestra
Entre el 1 de
enero de 2021 y el 31 de agosto de 2023, ingresaron 780 pacientes a la UCIP de
la institución. De ellos, 618 no cumplieron los criterios de inclusión, dos
tenían un esfuerzo terapéutico adecuado y uno fue derivado a otra institución.
Finalmente, 159 pacientes fueron incluidos en el análisis (Figura 1).
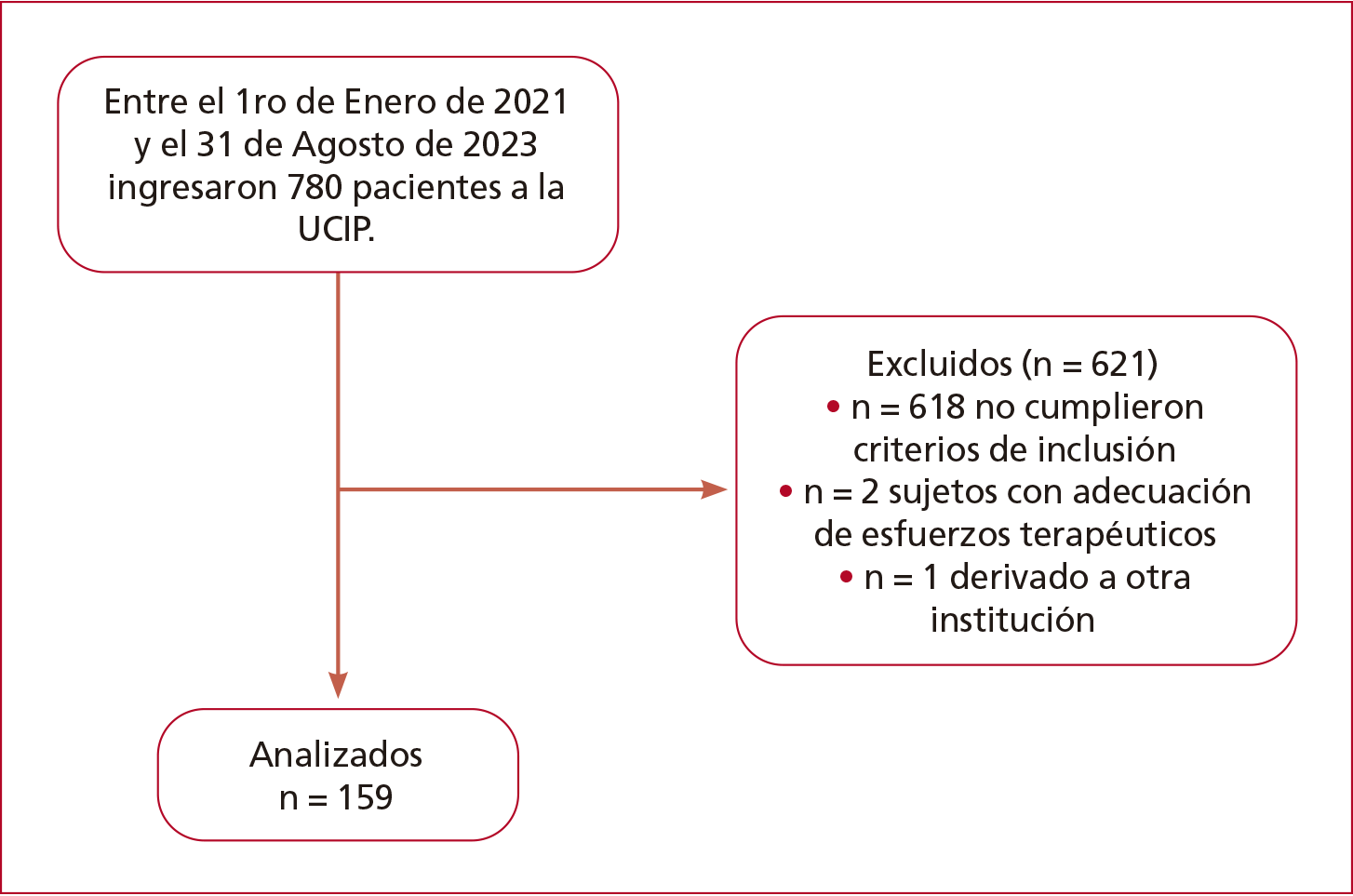
Figura 1. Diagrama de flujo de los participantes.
El 57,2% eran
varones y la mediana de edad de la muestra era de 15 (RIC 4-40) meses. El
diagnóstico de ingreso más prevalente fue IRA baja (139 casos, 87,4%). En más
del 60% de los casos, no se identificó ninguna comorbilidad y 27 (17%) tenían 2
o más comorbilidades, la más habitual era el nacimiento prematuro (22 casos,
13,8%), seguida de asma (11 casos, 6,9%) (Tabla 1).
|
TABLA 1 Características de los participantes al ingresar |
||||
|
Variables |
Todos |
Éxito de la
VNIi |
Fracaso de la VNIi |
p |
|
Sexo
masculino, n (%) |
91 (57,2) |
67 (59,3) |
24 (52,2) |
0,48 |
|
Edad,
mediana (RIC), meses |
15 (4-40) |
17 (4.5-42.5) |
10.5 (3-30.2) |
0,23 |
|
PIM,
mediana (RIC), puntaje |
0,37 (0,37-3,17) |
0,37 (0,14-3,17) |
1,22 (0,37-3,17) |
0,10 |
|
Diagnóstico
de ingreso, n (%) |
|
|
|
|
|
IRA baja |
139 (87,4) |
97 (85,8) |
42 (91,3) |
ref. |
|
Crisis
asmática |
14 (8,8) |
12 (10,6) |
2 (4,3) |
0,22 |
|
Otros |
6 (3,8) |
4 (3,5) |
2 (4,3) |
0,87 |
|
FiO2
al inicio de la VNIe, mediana (RIC), % |
0,4 (0,35-0,5) |
0,4 (0,35-0,5) |
0,5 (0,4-0,6) |
0,001 |
|
Saturación
al inicio de la VNIe, mediana (RIC), % |
98 (97-100) |
99 (98-100) |
98 (96-99) |
<0,01 |
|
SaFiO2 al inicio de VNIe, mediana
(RIC), % |
245 (190-277) |
245 (196-282) |
196 (163-246) |
<0,001 |
|
Cantidad
de comorbilidades, n (%) |
|
|
|
|
|
Ninguna |
107 (67,3) |
76 (67,3) |
31 (67,4) |
ref. |
|
Una |
25 (15,7) |
18 (15,9) |
7 (15,2) |
0,92 |
|
Dos o más |
27 (17) |
19 (16,8) |
8 (17,4) |
0,95 |
|
Comorbilidades,
n (%) |
|
|
|
|
|
Asma |
11 (6,9) |
9 (8) |
2 (4,3) |
0,51 |
|
Displasia broncopulmonar |
6 (3,8) |
3 (2,7) |
3 (6,5) |
0,36 |
|
Epilepsia |
7 (4,4) |
5 (4,4) |
2 (4,3) |
0,99 |
|
Nutrición enteral |
22 (13,8) |
13 (11,5) |
9 (19,6) |
0,21 |
|
Oncológicas |
3 (1,9) |
2 (1,8) |
1 (2,2) |
0,99 |
|
Cardiológicas |
5 (3,1) |
2 (1,8) |
3 (6,5) |
0,15 |
|
Neurodesarrollo |
8 (5) |
5 (4,4) |
3 (6,5) |
0,69 |
|
Genéticas |
9 (5,7) |
6 (5,3) |
3 (6,5) |
0,72 |
|
VNIi = ventilación
no invasiva inicial; VNIe = ventilación no invasiva electiva; RIC = rango
intercuartílico; PIM = índice de mortalidad pediátrica; FiO2 = fracción inspirada de oxígeno; SaO2/FiO2 =
relación entre la saturación de oxígeno y la FiO2; IRA = infección respiratoria aguda. |
||||
Rescates microbiológicos
En el momento
de ingresar a la institución, se realizaron 144 muestras microbiológicas
mediante diversas técnicas. A través de este proceso, se identificaron 245
casos de virus entre los cuales el Virus Sincitial Respiratorio (75 casos,
30,6%) y el Rhinovirus (76 casos, 31%) fueron los más frecuentes. En la Figura
2, se muestra la frecuencia de aparición de los distintos rescates
microbiológicos.
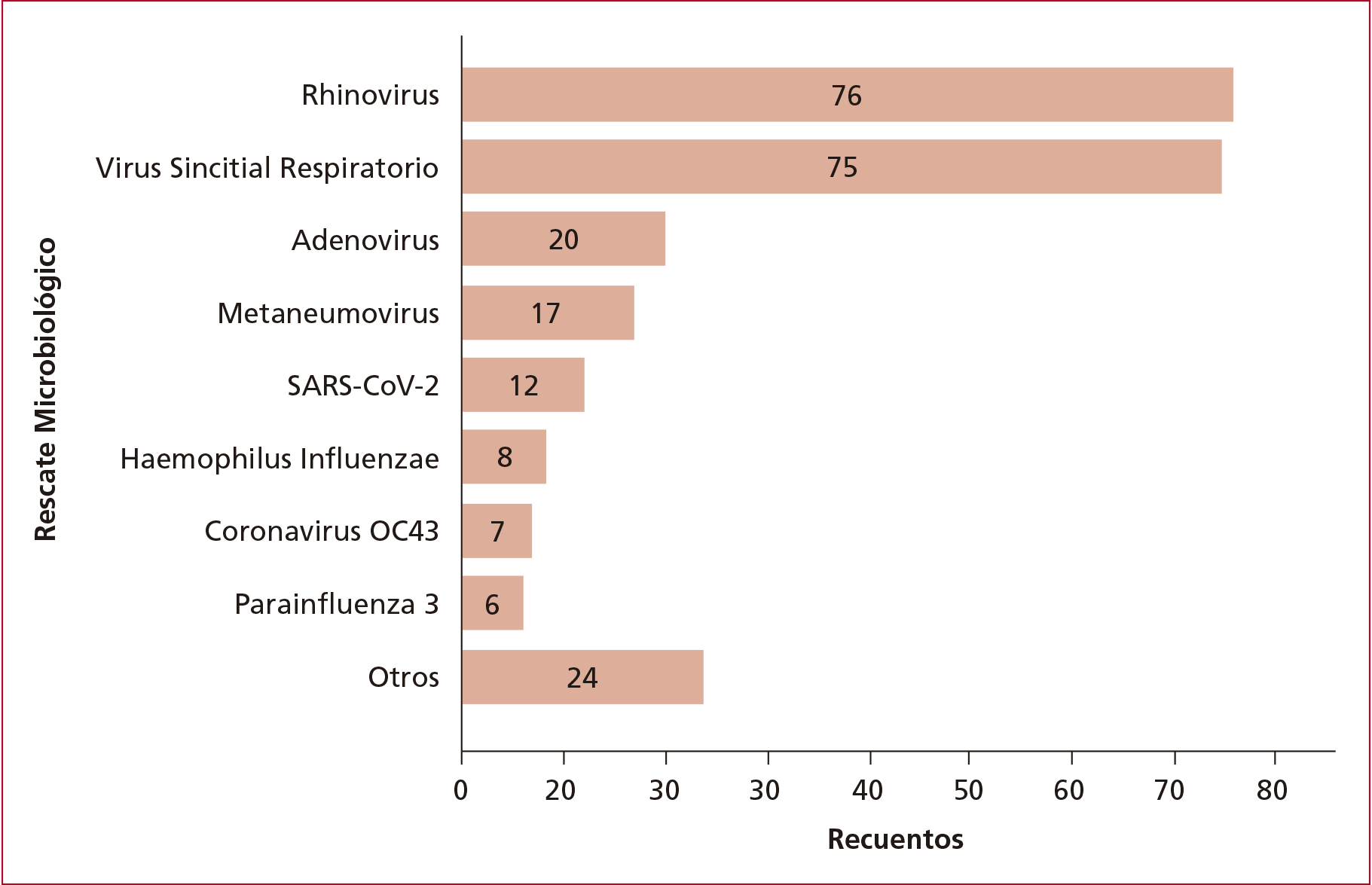
Figura 2. Frecuencia de rescate microbiológico.
Utilización de la VNIi
La mediana de
la duración de la VNIi fue de 2 días (RIC 2-4), con diferencias
estadísticamente significativas entre aquellos que respondieron a la
intervención (2 días, RIC 1-2) y aquellos que no (2 días, RIC 1-2) vs. 0 días
(RIC 0-0), respectivamente (p <0,001)]. El 95,6% (152 casos) recibió
sedación durante la implementación de la VNIi. Recibieron sedación 107 (94,7%)
del grupo de éxito de la VNIi y 45 (97,8%) de grupo de fracaso (p = 0,674).
Solo se produjo una muerte durante la estancia en la UCIP. Por último, la
mediana de días de internación fue de 8 (RIC 6-12). El grupo de éxito de la
VNIi permaneció internado durante 7 días (RIC 6-9), mientras que el grupo de
fracaso lo hizo durante 14.5 días (RIC 11-21) (p <0,001).
Factores asociados al éxito de la VNIi
Se realizaron
análisis univariados y multivariados de regresión logística con el objetivo de
identificar factores asociados al éxito de la VNIi (Tabla 2). De acuerdo con el
criterio de información de Akaike, se identificó un modelo final que incluyó a
las siguientes variables: índice de mortalidad pediátrica [OR 0,84 (IC95%
0,65-1,09); p = 0,20] y SaFiO2 al inicio de la VNIi [OR 1,01 (IC95%
1,00-1,02); p <0,01]. Solo la SaFiO2 se identificó de manera
estadísticamente significativa e independiente con el éxito de la VNIi. La
prueba de bondad de ajuste de Hosmer-Lemeshow resultó no significativa (p =
0,58) y el R2 de Nagelkerke fue de 0,11. El poder de clasificación evaluado
mediante el análisis del AUC resultó pobre [AUC 0,68 (IC95% 0,58-0,78); p =
0,001] (Figura 3).
|
Tabla 2 Análisis multivariado para factores
asociados al éxito de la ventilación no invasiva inicial |
|||||
|
Variables |
Univariado |
p |
|
Multivariado* |
p |
|
PIM |
0,83 (0,65-1,05) |
0,12 |
|
0,84 (0,65-1,09) |
0,20 |
|
SaFiO2 al inicio de la
VNIi |
1,01 (1,00-1,02) |
<0,01 |
|
1,01 (1,00-1,02) |
<0,01 |
|
VNIi = ventilación no invasiva inicial; PIM
= índice de mortalidad pediátrica; SaO2/FiO2 = relación entre la saturación de oxígeno y
la fracción inspirada de oxígeno; OR (odds ratio) = cociente de
posibilidades; IC95% = intervalo de confianza del 95%. *Selección paso a
paso con criterios de información de Akaike, AUC: 0,68 (0,58-0,78). |
|||||
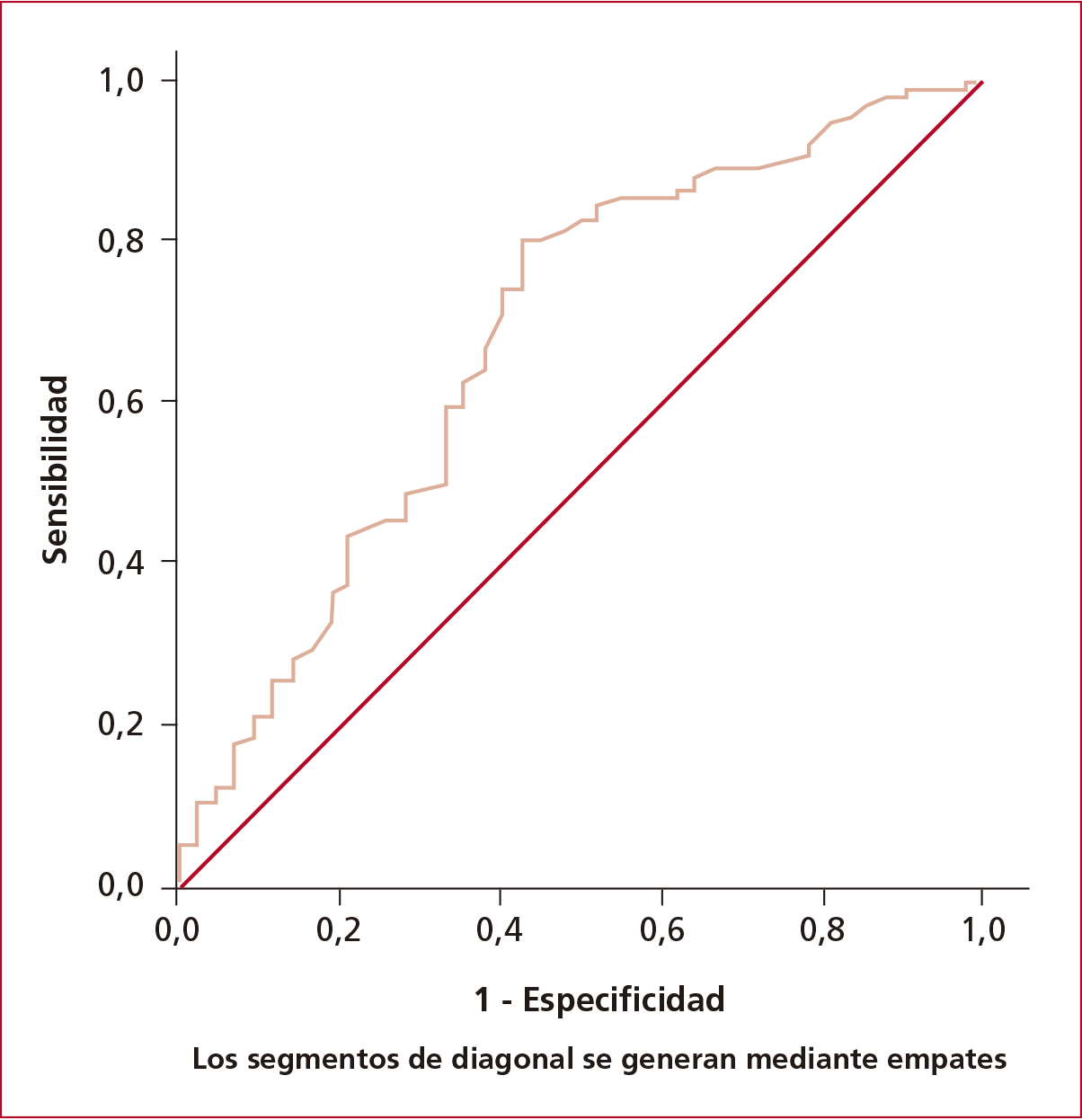
Figura 3. Curva ROC del modelo multivariado para la predicción de éxito de VNIi. El área bajo la curva (AUC) fue de 0.68 (IC 95%:0.58 – 0.78; p= 0.001), indicando una capacidad discriminativa pobre del modelo.
Discusión
El uso de ventilación
no invasiva como primera línea de tratamiento frente a la IRA ha ido creciendo
en la población pediátrica. Nuestra tasa de éxito asociada a la VNIi fue del
71,1%, es decir, 113 niños estuvieron internados sin requerimiento de
intubación y sus complicaciones asociadas. En un estudio de cohorte prospectivo
en pacientes con IRA y requerimiento de VNIi, Pons-Òdena et al obtuvieron
resultados similares: una tasa de éxito del 71%.17 En 2011, James et al publicaron una tasa de
éxito de la VNIi del 64%, y correlacionaron el fracaso con frecuencias
respiratorias iniciales más altas y mayor acidosis respiratoria.18 En el mismo año, en nuestro país, se publicó
un estudio descriptivo retrospectivo que analizó el éxito y las características
asociadas. La tasa de éxito informada fue del 52%.19 Si comparamos dicho valor con nuestro
resultado primario, el cual fue significativamente mayor, es probable que se
deba a varios factores, como mejor desarrollo de interfases y arneses para el
paciente, optimización del programa de los ventiladores, capacitación del
personal, entre otros. Por otra parte, en ambos estudios, se comparte que los
pacientes en quienes fracasó la VNIi y requirieron VMI tuvieron internaciones
más prolongadas.19
En pediatría,
la colocación de accesos arteriales para determinar gases en sangre conlleva un
proceso estrés para el niño, puede empeorar la mecánica ventilatoria, la
frecuencia respiratoria y la frecuencia cardíaca. La SaFiO2 es un
índice no invasivo, fácil de usar y disponible continuamente que se
correlaciona con la presión arterial de oxígeno/FiO2 (PAFI).20 En 2015, Pons-Òdena et al demostraron que una
SaFiO2 a las dos horas de iniciar la VNIi de 189 o menos se asociaba con el
fracaso.21 En contraposición a nuestro estudio, donde se
ha calculado la SaFiO2 al inicio de la implementación
terapéutica, pudimos obtener datos relevantes y se pudo considerar a la SaFiO2 una
variable independiente asociada al éxito de la VNIi. A pesar de no contar con
un punto de corte como valor predictivo de éxito, dicho resultado permite
interpretar que mejores SaFiO2 iniciales llevarán a mejores
resultados.
En nuestro
estudio, aquellos pacientes con una VNIi exitosa permanecieron menos días en la
UCIP que aquellos en quienes fracasó.
Durante los
últimos años, han ganado importancia los términos de familiarización y
humanización de la terapia intensiva, pero aun así, los días que los niños
permanecen internados se ven alejados de su hogar, de parte de su familia y de
su entorno habitual, a la vez que están sometidos a ruidos, luces permanentes,
procedimientos nocivos y expuestos a diferentes tipos de microorganismos, por
lo cual disminuir la estancia en la UCIP es uno de los objetivos más
importantes.22 No obstante, se ha demostrado que si bien la
VNI exitosa acorta la estancia hospitalaria, cuando fracasa la terapéutica y
requieren VMI tienen estancias más prolongadas que el promedio en general y
también puede aumentar la mortalidad cuando se retrasa la intubación.19,23
Como
limitaciones del estudio, al tratarse de un diseño retrospectivo, consideramos
tener faltante de datos o de variables posibles de analizar para obtener
mayores resultados. Si bien, en la práctica diaria, se utilizan diferentes
puntajes de gravedad para evaluar a los pacientes inicialmente, no contamos con
esos datos para poder correlacionarlos con el éxito o el fracaso. Por otra
parte, es probable que, debido a la naturaleza del tipo de estudio, no hayamos
encontrado factores asociados al fracaso de la VNIi, tales como frecuencia
respiratoria, frecuencia cardíaca o progresión del setting ventilatorio,
ya que no contamos con un seguimiento de registro de dichas variables luego de
iniciar la terapéutica como se ha demostrado en otros estudios.24,25
Conclusiones
La tasa de
éxito de la VNIi en pacientes de la UCIP de nuestra institución fue del 71,1%.
Dentro de las distintas variables analizadas la SaFiO2 inicial se
relaciona significativamente con el éxito de la VNIi.
Si bien se
necesitan estudios prospectivos para confirmar dichos hallazgos consideramos
que la VNIi es una práctica útil y confiable que evitó el ingreso de un alto
porcentaje de lactantes y niños con IRA a la intubación y VMI.
Agradecimiento
A todo el
equipo de kinesiología pediátrica, a los doctores García Roig, Alejandro Ellis
e Isabel Ayerza y a el Lic. Mauro Andreu.
Bibliografía
1.
Comité de Neumonología, Comité de Infectología, Comité de Medicina Interna Pediátrica, Comité de
Pediatría Ambulatoria y
Colaboradores. Recomendaciones para el manejo de las infecciones respiratorias
agudas bajas en menores de 2 años. Actualización 2021.
Arch Argent Pediatr 119(4): S171-S197. https://doi.org/10.5546/aap.2021.S171
2.
Vivero
P, Tarazona S, Cimadevilla R. Fracaso respiratorio agudo y crónico. Oxigenoterapia. Protoc diagn ter
pediatr 2017; 1: 369-399. Disponible en: https://www.aeped.es/sites/default/files/documentos/23_fracaso_respiratorio.pdf
3.
Agency
for Healthcare Research and Quality. Healthcare Cost and Utilization Project
(HCUP) Nationwide Emergency Department Sample (NEDS). Rockville, MD: Agency for
Healthcare Research and Quality; 2008.
4.
Farias
JA, Fernández A, Monteverde, et al, Latin-American Group for
Mechanical Ventilation in Children. Mechanical ventilation in pediatric
intensive care units during the season for acute lower respiratory infection: a
multicenter study. Pediatr Crit Care Med 2012; 13(2): 158-164. https://doi.org/10.1097/PCC.0b013e3182257b82
5.
Essouri
S, Chevret L, Durand P, et al. Noninvasive positive pressure ventilation: Five
years of experience in a pediatric intensive care unit. Pediatr Crit Care Med
2006; 7(4): 329-334. https://doi.org/10.1097/01.PCC.0000225089.21176.0B
6.
Yañez L, Yunge M, Emilfork M, et al. A prospective,
randomized, controlled trial of noninvasive ventilation in pediatric acute
respiratory failure. Pediatr Crit Care Med 2008; 9(5): 484-489. https://doi.org/10.1097/PCC.0b013e318184989f
7.
Barros da
Silva Lins AR, Menezes Becerra Duarte MC, Barboza de Andrade L. Noninvasive
ventilation as the first choice of ventilatory support in children. Rev Bras
Ter Intensiva 2019; 31(3): 333-339. https://doi.org/10.5935/0103-507X.20190045
8.
Nørregaard O. Noninvasive ventilation in children. Eur Respir
J 2002; 20(5): 1332-1342. https://doi.org/10.1183/09031936.02.00404802
9.
Prado
F, Godoy MA, Godoy M, Boza ML. Ventilación no
invasiva como tratamiento de la insuficiencia respiratoria aguda en Pediatría. Rev
Méd Chile 2005; 133(5): 525-533. https://doi.org/10.4067/S0034-98872005000500003
10. Teague G. Noninvasive ventilation in the pediatric
intensive care unit for children with acute respiratory failure. Pediatr
Pulmonol 2003; 35(6): 418-426. https://doi.org/10.1002/ppul.10281
11. Lule
Morales M, de la Rosa Rodríguez A, Robledo Pascual J,
Narváez Porras O, Niebla Álvarez B. Eficiencia de la ventilación mecánica no
invasiva en pacientes pediátricos con insuficiencia
respiratoria aguda. Rev Inst Nal Enf Resp Mex 2004; 17(3): 181-191. Disponible
en: https://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S0187-75852004000300004
12. Loh L, Chan Y, Chan I. Noninvasive ventilation in
children: a review. J Pediatr (Rio J) 2007; 83(2 Suppl): S91-99. https://doi.org/10.2223/JPED.1613
13. Tal A,
Ravilski C, Yohai D, et al. Dexamethasone
and salbutamol in the treatment of acute wheezing in infants. Pediatrics
1983; 71: 13. PMID: 6129609
14. Wood D, Downes J, Lecks H. A clinical scoring system
for diagnosis of respiratory failure. Am J Dis Child 1972; 123: 227-228. https://doi.org/10.1001/archpedi.1972.02110090097011
15. Akaike H. Statistical predictor identification. Ann
Inst Math Stat 1970; 22: 203-217. https://doi.org/10.1007/BF02506337
16. Fischer JE, Bachmann LM, Jaeschke R. A readers’ guide to the interpretation of diagnostic test
properties: clinical example of sepsis. Intensive Care Med 2003; 29(7):
1043-1051. https://doi.org/1010.1007/s00134-003-1761-8
17. Pons-Òdena M, Medina A, Modesto V, et al. ¿Cuáles son
los factores predictores de fracaso de ventilación no
invasiva más fiables en una unidad de
cuidados intensivos pediátricos? An Pediatr (Barc) 2019; 91(5): 307-316. https://doi.org/10.1016/j.anpedi.2019.01.013
18. James CS, Hallewell CPJ, James DPL, Wade A, Mok QQ.
Predicting the success of non-invasive ventilation in preventing intubation and
re-intubation in the paediatric intensive care unit. Intensive
Care Med 2011; 37: 1994-2001. https://doi.org/10.1007/s00134-011-2386-y
19. Bonora JP,
Frachia D, García M, et al. Ventilación no invasiva en cuidado Intensivo Pediátrico, cuatro años de
experiencia. Arch Argent Pediatr 2011; 109(2): 124-128. Disponible en: https://www.scielo.org.ar/scielo.php?script=sci_arttext&pid=S0325-00752011000200006
20. Mayordomo
Colunga J, Pons M, López Y, et al. Predicting non-invasive ventilation failure in
children from the SpO2/FiO2 (SF) ratio. Intensive Care Med 2013; 39(6):
1095-1103. https://doi.org/10.1007/s00134-013-2880-5
21. Pons-Òdena M, Palanca D, Modesto V, et al. SpO2/FiO2 as a predictor of
non-invasive ventilation failure in children with hypoxemic respiratory
insufficiency. J
Pediatr Intensive Care 2013; 2: 111-119. https://doi.org/10.3233/PIC-13059
22. Toobe M. Síndrome post cuidados intensivos en pediatría. Rev Fac Cien Med Univ Nac Córdoba 2021; 78(4): 408-414. Disponible en: https://revistas.unc.edu.ar/index.php/med/article/view/32809
23. Ganu SS, Gautam A, Wilkins B, Egan J. Increase in use
of non-invasive ventilation for infants with severe bronchiolitis is associated
with decline in intubation rates over a decade. Intensive Care Med 2012; 38(7):
1177-1183. https://doi.org/10.1007/s00134-012-2566-4
24. Alonso B, Boulay M, Dall Orso P, et al. Ventilación no invasiva en menores de dos años internados en sala con infección respiratoria aguda baja. Posibles factores
predictivos de éxito y de fracaso. Arch
Pediatr Urug 2012; 83(4): 250-255. Disponible en: http://www.scielo.edu.uy/scielo.php?pid=S1688-12492012000400003&script=sci_abstract
25. Kneyber
MCJ, de Luca D, Calderini E, et al. Recommendations
for mechanical ventilation of critically ill children from the Paediatric
Mechanical Ventilation Consensus Conference (PEMVECC). Intensive
Care Med 2017; 43(12): 1764-1780. https://doi.org/10.1007/s00134-017-4920-z)