Anafilaxia por sulfato de magnesio: reporte de
un caso
[Magnesium sulfate anaphylaxis: a case report]
Jaqueline P. Tipas
Cuaspud,a Armando H. M. Yee
Acendra,a Álvaro A. Montenegro
Apraez,b* David E. Cruz
Arevalo,c Luis E. Acevedo
Patiño,d Luis A. Bustamante
Cristanchob
a Residente en Medicina de Urgencias, 3.er año, Pontificia Universidad
Javeriana, Cali, Colombia
b Especialista en Cuidado Intensivo, Docente del
Programa de Medicina de Urgencias, Pontificia Universidad Javeriana, Cali,
Colombia
c Fellow en Cuidado Intensivo, Universidad del Valle,
Colombia
d Médico asistencial Cuidado Intensivo, Clínica
Imbanaco, Cali, Colombia
* Correspondencia: alvaro.montenegro@javeriana.edu.co
Los autores no
declaran conflictos de intereses.
https://doi.org/10.64955/jratiy2025x926
Resumen
El sulfato de magnesio se utiliza en el
tratamiento de las crisis asmáticas severas como una terapia adyuvante debido a
su capacidad para actuar como un broncodilatador secundario a la inhibición de
la contracción del músculo liso bronquial; sin embargo, su administración puede
provocar efectos adversos, como hiporreflexia, hipotensión, rubor, sensación de
calor e hipotermia; la anafilaxia es una reacción adversa excepcional que se ha
publicado en tres oportunidades. Presentamos un caso de anafilaxia por sulfato
de magnesio durante una crisis asmática severa y que representa el cuarto caso
comunicado.
Palabras clave: Anafilaxia; sulfato de magnesio; espasmo
bronquial; estado asmático; reporte de caso.
Abstract
Magnesium sulfate is used in the treatment of
severe asthmatic crisis as an adjuvant therapy due to its capacity to act as a
bronchodilator secondary to the inhibition of bronchial smooth muscle
contraction; however, its administration can cause adverse effects, such as
hyporeflexia, hypotension, flushing, sensation of heat and hypothermia.
Anaphylaxis is an exceptional adverse reaction that has been reported in the
literature on 3 occasions; we present a case of anaphylaxis due to magnesium
sulfate during a severe asthmatic crisis, representing the fourth case reported
in the literature.
Keywords: Anaphylaxis; magnesium sulfate; bronchial spasm;
status asthmaticus; case report.
Introducción
La anafilaxia por sulfato de magnesio es excepcional, se han publicado tres casos que tuvieron una evolución favorable después del manejo con adrenalina y esteroide sistémico.1-3
Este artículo tiene como objetivo proporcionar un análisis de causalidad de la reacción adversa descrita, así como dar a conocer un excepcional riesgo durante el uso de sulfato de magnesio.
Caso clínico
Mujer de 75 años, con hipertensión arterial controlada, asma desde la infancia, con episodios de exacerbación clasificados como leves sin necesidad de hospitalización. Consultó al servicio de urgencias por cuadro de 12 horas de disnea rápidamente progresiva. Como único factor de exacerbación se documentó la ausencia del uso de un fármaco controlador del asma (corticoides). En el examen físico, tenía signos de broncoespasmo, desaturación (SatO2 76%), tiraje subcostal y disminución del murmullo vesicular, por lo cual se indicó el uso de inhaladores de dosis media con un agonista ß2 de acción corta (salbutamol) y un antagonista muscarínico (ipratropio); además, se agregó un esteroide sistémico por vía intravenosa (metilprednisolona).
Ante la falta de respuesta del broncoespasmo y la disnea persistente que le impedía completar oraciones, se decidió comenzar a administrar sulfato de magnesio (presentación en solución inyectable de 2 g de MgSO4 en 100 ml); sin embargo, a los 20 minutos de iniciar el medicamento, apareció un eritema que comenzó en la cara y se extendió rápidamente al cuello, el tórax y las extremidades, acompañado de prurito y deterioro de la función respiratoria dado por la desaturación, el uso de musculatura accesoria y la tos persistente.
Debido a la evolución tórpida se decide asegurar la vía aérea e iniciar el soporte ventilatorio mecánico invasivo, suspender la infusión de sulfato de magnesio y trasladarla a la unidad de cuidados intensivos.
Inicialmente se indica un ajuste de la dosis de sedación, analgésicos e inicio de relación neuromuscular (cisatracurio). Los primeros estudios con un panel molecular de vías respiratorias muestran una coinfección por metaneumovirus humano como posible precipitante de la crisis asmática; no obstante, los cambios clínicos descritos tras la administración de sulfato de magnesio se consideraron como una posible anafilaxia; por esta razón, se suspendió su uso en los días posteriores.
Durante la evolución, se registró un trastorno leve de la oxigenación, acidemia respiratoria debido a la elevación de la presión de dióxido de carbono de manera progresiva (Tabla). Se consideró una estrategia de ventilación mecánica protectora con parámetros de hipercapnia permisiva; asimismo, se ajustó la dosis de esteroide sistémico con metilprednisolona (60 mg, cada 6 h), se optimizaron las dosis de salbutamol y bromuro de ipratropio, se agregaron budesonida formoterol (Rapihaler® 160/4,5 µg - dosis de 8 puff cada 4 h), y loratadina y montelukast.
Tabla
Estudios de seguimiento*
|
Gases
arteriales |
pH |
pCO2 (mmHg) |
pO2 (mmHg) |
HCO3- (mEq/l) |
SatO2 (%) |
Lactato (mmol/l) |
|
Ingreso |
7,40 |
44,4 |
65,1 |
27 |
94,3 |
2,3 |
|
Día 1 am |
7,39 |
44 |
147 |
26 |
99 |
1,2 |
|
Día 1 pm |
7,33 |
53,2 |
173,1 |
27,7 |
99,3 |
1,27 |
|
Día 2 pm |
7,32 |
56,7 |
77,4 |
29 |
96,4 |
1,38 |
|
Día 2 |
7,26 |
69,5 |
91 |
30,8 |
96,8 |
2,2 |
|
Día 3 |
7,33 |
57,2 |
73,9 |
29,7 |
95,5 |
2,2 |
|
Día 3 |
7,24 |
76,4 |
81,1 |
32,2 |
94,8 |
|
* Nótese el deterioro progresivo en el estado ácido base relacionado con el incremento de la pCO2.
Ante el deterioro clínico, se consideró realizar una tomografía computarizada de tórax que reveló bronquiectasias cilíndricas y engrosamiento de paredes bronquiales especialmente en el hilio, que son típicas en los pacientes con infección por metaneumovirus (Figura).
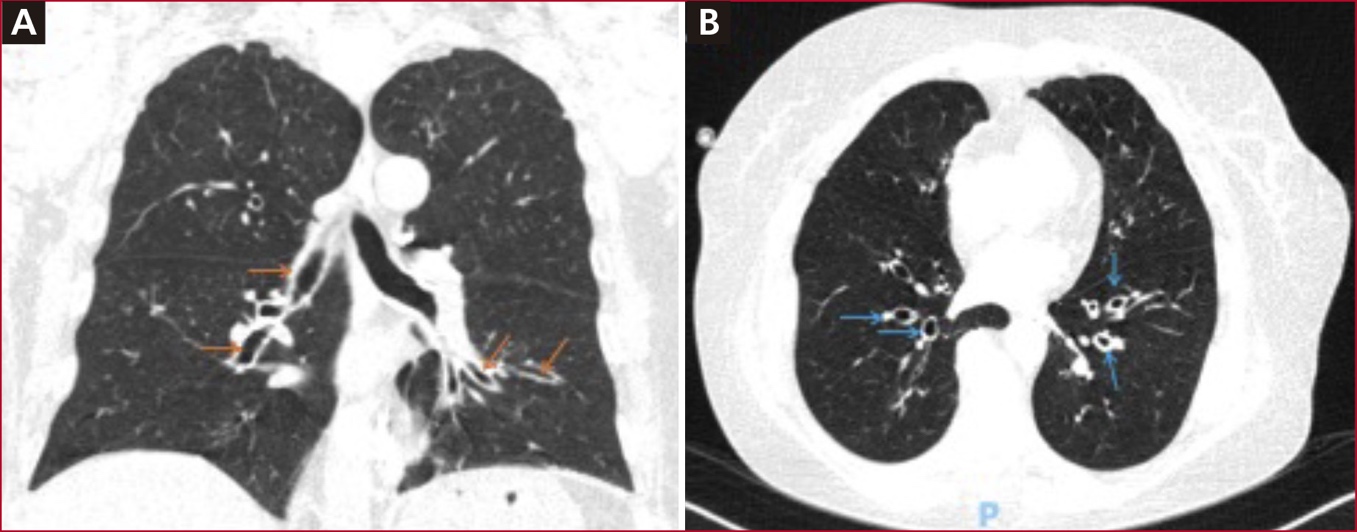
Figura. Tomografía de tórax. A. Pequeñas bronquiectasias cilíndricas en el aspecto medial de ambos lóbulos inferiores (flechas naranjas) especialmente en el pulmón izquierdo. B. Ligero engrosamiento de las paredes bronquiales (flechas azules).
La pobre respuesta clínica al manejo médico descrito y la progresión de la acidemia respiratoria marcada a partir de las 48 horas (Tabla) llevaron a iniciar la sedación con isoflurano a través del sistema AnaConDa® (anaestethetic conserving device) en un intento de disminuir la resistencia de las vías aéreas, al tiempo que se mantuvo el uso de analgésicos opiáceos y la relajación neuromuscular debido a la persistencia del broncoespasmo; sin embargo, la evolución fue tórpida debido a la inestabilidad hemodinámica progresiva que precipitó un shock sin respuesta a las catecolaminas en quien se consideró una probable falla ventricular derecha; no se consideró la oxigenación por membrana extracorpórea (ECMO) por criterio de exclusión de la edad de la paciente. Finalmente sufrió un paro cardiorrespiratorio que no respondió a las maniobras avanzadas de reanimación y falleció a las 72 horas de ingresar en la institución.
Discusión
Según la Guía Global para el Asma,1 las características de los pacientes que sufren una crisis asmática severa son: imposibilidad para pronunciar oraciones (debido a la disnea severa), taquipnea >30 respiraciones por minuto, taquicardia >120 latidos por minuto, uso de músculos accesorios, presión arterial de oxígeno <60 mmHg, presión arterial de CO2 >50 mmHg y un pico flujo espiratorio <50%. El esquema terapéutico sugerido puede incluir broncodilatadores de corta acción, corticoides sistémicos, oxigenoterapia y, si la respuesta es inadecuada, se sugiere el uso de sulfato de magnesio.4-6
En el caso presentado, la persistencia de la disnea que le impedía pronunciar oraciones permite clasificar la crisis como severa, por lo que se puede inferir que el uso de sulfato de magnesio se considera adecuado en este contexto clínico.
Por otra parte, tras la administración de sulfato de magnesio, el curso clínico y la severidad de la crisis se agravaron debido al deterioro de la función respiratoria, con requerimiento del músculos accesorios y necesidad de ventilación mecánica invasiva, lo anterior sumado a la reacción eritematosa de rápida progresión y la tos de reciente comienzo permitió sospechar una anafilaxia por sulfato de magnesio.
En la bibliografía científica actual, no
existe una definición universal de anafilaxia; sin embargo, la World Allergy
Organization propuso una revisión de los criterios sobre anafilaxia sugiriendo
dos puntos importantes, donde se requiere, al menos, cumplir uno para
considerar un caso probable de anafilaxia, estos son:7
1. Inicio agudo de minutos a horas con compromiso de la piel y el tejido mucoso.
2. Episodio agudo de hipotensión o broncoespasmo o afectación laríngea.
En nuestra paciente, se cumplen los dos puntos que estipula la World Allergy Organization; además, es importante mencionar que, debido a la relación temporal (deterioro posterior a la administración de sulfato de magnesio), el deterioro del broncoespasmo, asociado a lesiones cutáneas eritematosas típicas, sugieren el curso de anafilaxia por sulfato de magnesio.
En la revisión bibliográfica, se encontramos tres casos de reacciones anafilácticas secundarias a sulfato de magnesio.1,3 Los pacientes tienen síntomas o signos, como rubor facial, prurito, hipotensión, taquicardia, taquipnea, estridor e hipoxemia; también niveles séricos bajos de magnesio (inferiores al rango de referencia: 1,6-2,6 mg/dl); las reacciones variaron en el tiempo de presentación, desde 20 minutos hasta 2 horas después de la administración del medicamento, todos los pacientes respondieron al manejo con adrenalina, corticoides sistémicos y antihistamínicos; no se comunicaron muertes, a diferencia de lo que ocurrió con nuestra paciente.
Los factores que podrían estar relacionados con la muerte incluyen la disminución en la reserva fisiológica (debido a la edad avanzada), la remodelación de las vías respiratorias (especialmente por el tiempo de evolución del asma), la comorbilidad cardiovascular (hipertensión arterial), la crisis asmática que fue agravada por una probable reacción anafiláctica secundaria al sulfato de magnesio y finalmente la omisión en el uso de adrenalina como parte del manejo de la anafilaxia, que, según algunas publicaciones, se ha relacionado con un incremento de desenlaces fatales.
El caso presentado sugiere el curso con una probable reacción anafiláctica, debido a la presentación aguda de deterioro del broncoespasmo, la reacción cutánea eritematosa (erupción urticariana) y el deterioro de la función respiratoria que condujeron a la insuficiencia respiratoria después de la administración de sulfato de magnesio, lo que cumple con los criterios para anafilaxia según lo expuesto por la World Allergy Organization y la Australian Society of Immunology and Allergy.8,9
Cabe destacar que existe plausibilidad biológica en el evento de anafilaxia secundaria a la administración de sulfato de magnesio debido las descripciones publicadas de casos previos.1-3 El análisis de causalidad de esta reacción adversa tiene una puntuación de 3 en la escala de Naranjo, lo que clasifica el presente caso como una reacción anafiláctica posible, secundaria a sulfato de magnesio, y representa el cuarto caso publicado.
Conclusiones
El sulfato de magnesio está indicado en el manejo de las crisis asmáticas severas sin respuesta al tratamiento inicial. Durante su administración, se debe estar atento a las reacciones adversas medicamentosas, la anafilaxia es la que plantea un mayor riesgo de muerte. Se ha presentado la cuarta descripción de anafilaxia por sulfato de magnesio.
Bibliografía
1. Coan N, Schiers K, Espinosa J, Lucerna A. Case report:
anaphylactic reaction to magnesium sulfate (2023). Rowan-Virtua Research Day.
115. Disponible
en: https://rdw.rowan.edu/stratford_research_day/2023/may4/115
2. Karki
S, Toofantabrizi M, Basnet S. Magnesium sulfate-induced anaphylaxis: a case report and review of the
literature. Cureus 2023; 15(9): e46071. https://doi.org/10.7759/cureus.46071
3.
Al-Fares
AA, Abdulmalek KA, Al-Herz W. Magnesium sulfate-induced nonallergic
anaphylaxis. Ann Allergy Asthma Immunol 2007; 98(3): 303. https://doi.org/10.1016/S1081-1206(10)60724-7
4.
Garner O,
Ramey JS, Hanania NA. Management of life-threatening asthma: severe asthma
series. Chest 2022; 162(4): 747-756. https://doi.org/11.1016/j.chest.2022.02.029
5.
Talbot T,
Roe T, Dushianthan A. Management of acute life-threatening asthma exacerbations
in the intensive care unit. Appl Sci (Basel) 2024; 14(2): 693. https://doi.org/10.3390/app14020693
6.
Guía Española para
el Manejo del Asma (GEMA) 5.4 [Consulta: 5 de septiembre, 2024]. Disponible en:
https://www.separ.es/node/1812
7.
Cardona
V, Ansotegui IJ, Ebisawa M, et al. World
Allergy Organization Anaphylaxis Guidance 2020. World Allergy Organ J 2020;
13(10): 100472. http://doi.org/10.1016/j.waojou.2020.100472
8.
Australian
Commission on Safety and Quality in Health Care. Acute Anaphylaxis Clinical
Care Standard 2021. Disponible en: safetyandquality.gov.au/standards/clinical-care-standards/acute-anaphylaxis-clinical-care-standard
9.
Global
Strategy for Asthma Management and Prevention, 2024. [Consulta:
5 de septiembre, 2024]. Disponible en: https://ginasthma.org/2024-report/