Tormenta arrítmica por crisis tirotóxica
inducida por amiodarona
[Arrhythmic Storm Induced by Thyrotoxicosis
Secondary to Amiodarone]
Jessica Giménez
Lecina,a* Laura Ventura
Prado,a Miriam Royo Álvarez,a Eva Sampedro
Calavia,a Pilar García
Mangas,b Ana Esteban Molinab
a MIR de Medicina Intensiva, Hospital
Universitario Miguel Servet, Zaragoza, España
b Facultativo Especialista Adjunto en Medicina
Intensiva, Hospital Universitario Miguel Servet, Zaragoza, España
* Correspondencia: jekalngs90@gmail.com
Las autoras no
declaran conflictos de intereses.
https://doi.org/10.64955/jratiy2025x898
Resumen
La crisis tirotóxica es una complicación grave
que puede precipitar inestabilidad hemodinámica y tormenta arrítmica en
pacientes con cardiopatía estructural. La amiodarona, un antiarrítmico de uso
frecuente, es un desencadenante reconocido de tirotoxicosis, y esto agrava el
manejo en individuos con insuficiencia cardíaca avanzada. Se describe el caso
de un hombre de 52 años que sufría de miocardiopatía dilatada y tenía un
desfibrilador con terapia de resincronización cardíaca, quien desarrolló una
crisis tirotóxica inducida por amiodarona en el contexto de una tormenta
arrítmica resistente. Se le administró un tratamiento intensivo con
betabloqueantes, inhibidores de la síntesis hormonal y manejo antiarrítmico
escalonado, con el que se logró la estabilización hemodinámica. Este caso resalta la importancia del
diagnóstico precoz de la tirotoxicosis inducida por amiodarona y la necesidad
de un abordaje multidisciplinario para mejorar la estabilidad clínica y el
pronóstico, especialmente en pacientes con insuficiencia cardíaca avanzada.
Palabras clave: Amiodarona; crisis tiroidea; arritmia
cardíaca; insuficiencia cardíaca; trasplante cardíaco.
Abstract
Thyrotoxic crisis is a serious complication that
can precipitate hemodynamic instability and arrhythmic storm in patients with
structural heart disease. Amiodarone, a commonly used antiarrhythmic, is a
recognized trigger of thyrotoxicosis, which
complicates management in patients with advanced heart failure. We describe the
case of a 52-year-old man with dilated
cardiomyopathy and a defibrillator with cardiac resynchronization therapy. He
developed amiodarone-induced thyrotoxic crisis in the context of refractory
arrhythmic storm. He was given intensive treatment with beta-blockers, hormone
synthesis inhibitors, and stepped antiarrhythmic management, which achieved
hemodynamic stabilization. This case highlights the importance of early
diagnosis of amiodarone-induced thyrotoxicosis and the need for a
multidisciplinary approach to improve clinical stability and prognosis,
especially in patients with advanced heart failure.
Keywords: Amiodarone; thyroid crisis; cardiac arrhythmia;
heart failure; heart transplant.
Introducción
La crisis tirotóxica es un cuadro
potencialmente mortal caracterizado por una exacerbación severa del
hipertiroidismo que puede desencadenar una disfunción multiorgánica y
descompensación cardiovascular. Si se demora el tratamiento, la tasa de
mortalidad alcanza el 20-30%.1 Su aparición en pacientes con cardiopatía
estructural representa un desafío terapéutico aún mayor, sobre todo, si tienen
dispositivos de terapia de resincronización cardíaca y antecedentes de
arritmias ventriculares malignas.2
Uno de los factores desencadenantes más
reconocidos de la disfunción tiroidea en pacientes con enfermedad
cardiovascular es la amiodarona, un antiarrítmico ampliamente utilizado en el
manejo de taquiarritmias resistentes. Su alto contenido de yodo y sus efectos
directos sobre la glándula tiroides pueden dar lugar a disfunciones tanto hipo
como hipertiroideas, incluidas las formas graves, como la tirotoxicosis
inducida por amiodarona.3 Esta entidad clínica está relacionada con un
incremento en la mortalidad, particularmente en pacientes con insuficiencia
cardíaca avanzada y tormenta arrítmica, donde la inestabilidad eléctrica puede
comprometer, de manera crítica, el pronóstico.4
Se presenta el caso de un paciente con miocardiopatía dilatada que tenía un desfibrilador automático implantable con terapia de resincronización cardíaca, y desarrolló una crisis tirotóxica en el contexto de una tormenta arrítmica resistente al tratamiento convencional, por lo que requirió el ingreso en la Unidad de Cuidados Intensivos.
Caso clínico
Hombre de 52 años, sin factores de riesgo cardiovascular, con antecedentes de bocio simple eutiroideo. Como antecedentes cardiológicos se destacaba una estenosis aórtica congénita operada mediante comisurotomía a los 9 años, que evolucionó a una doble lesión aórtica, por lo que había sido sometido a una sustitución valvular aórtica con prótesis mecánica y ampliación de la raíz aórtica, en 2010. Tuvo un deterioro funcional progresivo, con disfunción de la prótesis valvular e insuficiencia mitral secundaria.
En 2019, se desestimó una nueva cirugía de recambio valvular y se decidió colocarle un desfibrilador automático implantable con terapia de resincronización cardíaca.
El paciente ingresó por una tormenta arrítmica en julio de 2022, y se iniciaron los trámites de estudios previos al trasplante cardíaco. Se realizaron hasta 4 ablaciones de sustratos arrítmicos sin éxito, con inducción posterior de nuevas taquicardias ventriculares con diferentes ejes y morfologías, y se mantuvo en tratamiento habitual domiciliario con amiodarona 200 mg/día y bisoprolol.
En sucesivos
controles, se observó una caída de la fibrilación auricular y se aumentó la
dosis de amiodarona para controlarla. A los pocos días, consultó por disnea y
palpitaciones. Se detectó fibrilación auricular con respuesta ventricular
rápida y signos de insuficiencia cardíaca congestiva que se resolvieron tras la
cardioversión y el tratamiento depletivo.
La ecocardioscopia reveló una dilatación
severa de la aurícula izquierda y ligera de la aurícula derecha, un ventrículo
izquierdo severamente dilatado con disfunción sistólica moderada (FEVI 38%, SLG
-13%), un ventrículo derecho ligeramente dilatado con disfunción sistólica
moderada, una prótesis valvular aórtica con signos de estenosis con parámetros
en el límite de la severidad; insuficiencia aórtica ligera, insuficiencia
mitral moderada por dilatación del anillo y tenting predominante del
velo posterior e hipertensión pulmonar severa (Figura 1).
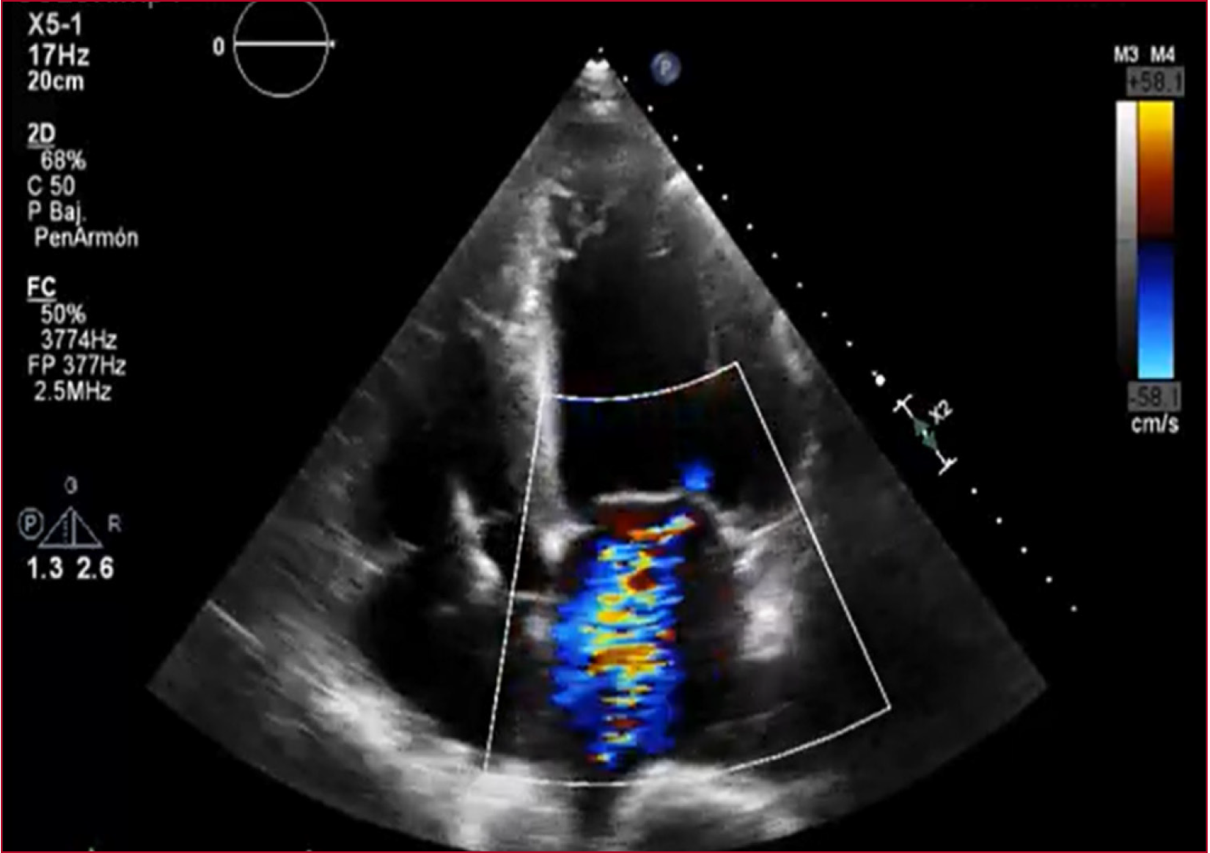
Figura 1. Ecocardioscopia transtorácica en Doppler color, 4 cámaras. Se observa insuficiencia mitral moderada.
A las 48 h, acudió tras varias descargas del desfibrilador automático implantable con terapia de resincronización cardíaca. En este, se observaba fibrilación auricular con episodios de taquicardia ventricular que no cedían con la terapia de estimulación antitaquicardia y sí con descargas apropiadas. Fue hospitalizado bajo tratamiento con amiodarona por vía intravenosa. Durante su estancia, sufrió episodios repetidos de taquicardia ventricular monomorfa sostenida, pese al tratamiento antiarrítmico con procainamida en perfusión continua e inestabilidad hemodinámica (Figura 2).
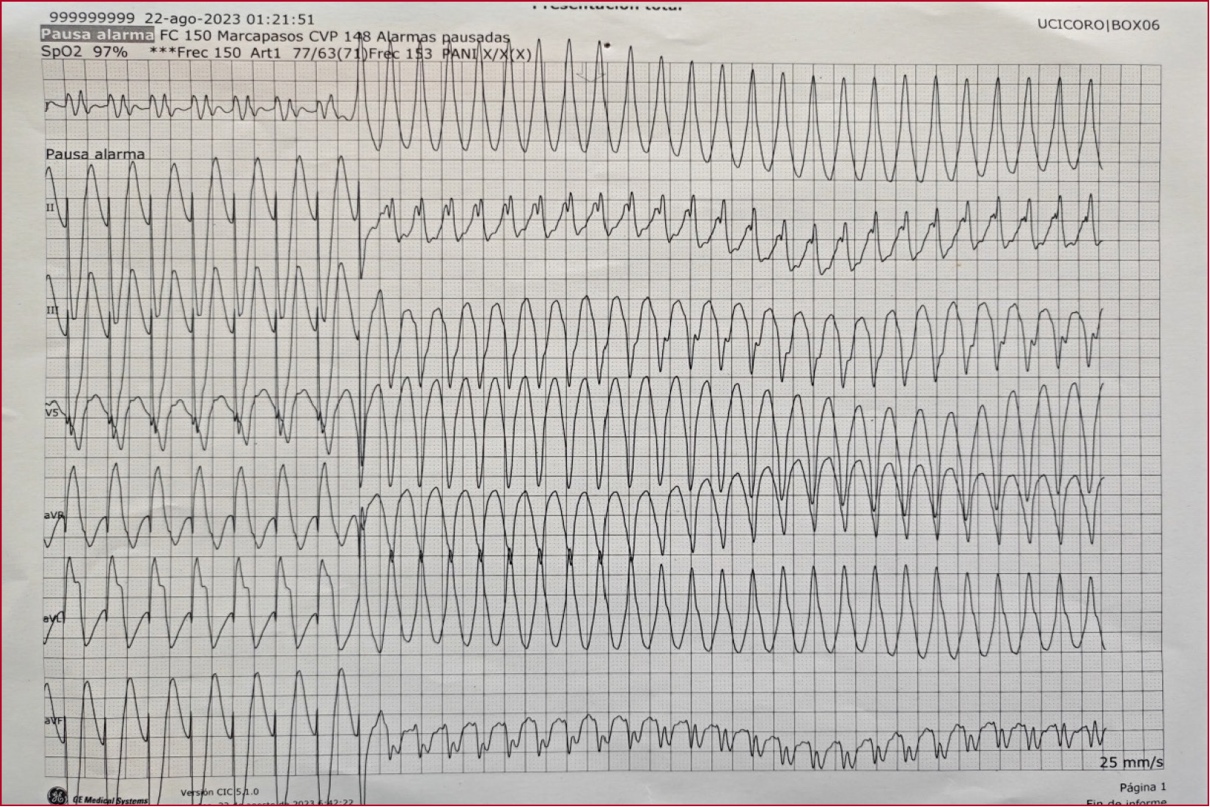
Figura 2. Electrocardiograma de 12 derivaciones que muestra una taquicardia ventricular monomorfa sostenida.
En los análisis de control, se destacaba una T3 de 23 nmol/l.
La ecografía tiroidea reveló un aumento difuso de la glándula tiroides y un incremento de su vascularización, compatible con una situación de tirotoxicosis.
Se administró un tratamiento específico ante la crisis tirotóxica con esmolol en perfusión continua (100-150 µg/kg/min), perclorato potásico 100 mg, cada 5 h; dexametasona 4 mg, cada 6 h y tiamazol 15 mg cada 8 horas. Como tratamiento antiarrítimico se indicó procainamida a dosis crecientes de hasta 4 g al día y, ante el inicial mal control de las alteraciones del ritmo, se inició la sedoanalgesia con cloruro mórfico 20 mg/día y dexmedetomidina como simpaticolítico a dosis de 0,4-0,6 µg/kg/minuto.
De esta forma
y, hasta conseguir el control progresivo de los niveles de T3, se logró
manejar la situación de inestabilidad eléctrica a los 4 días del ingreso. Esto
permitió sustituir la procainamida por mexiletina 167 mg, cada 24 h, el esmolol
por propranolol 40 mg, cada 6 h y añadir clonidina 0,15 mg, cada 12 h como
simpaticolítico en sustitución de la dexmedetomidina, con el fin de suspender
todo tratamiento intravenoso. El paciente evolucionó favorablemente y pudo
continuar con el tratamiento en sala de internación.
Discusión
La tirotoxicosis inducida por amiodarona
es una complicación poco frecuente, pero grave, que puede surgir en pacientes
tratados con este fármaco, especialmente aquellos que sufren una cardiopatía
estructural o arritmias ventriculares malignas. La interacción entre la
amiodarona y el sistema endocrino, junto con la predisposición cardiovascular
de estos pacientes, crea un cuadro clínico que representa un desafío
diagnóstico y terapéutico.1,2
La amiodarona es conocida por inducir
dos formas de tirotoxicosis: la tipo 1 y la tipo 2. La tirotoxicosis tipo 1 se
observa en pacientes con enfermedad tiroidea subyacente, y se caracteriza por
una sobreproducción de hormonas tiroideas debido al exceso de yodo
proporcionado por la amiodarona, mientras que el tipo 2 se produce por una
tiroiditis destructiva con liberación masiva de hormonas tiroideas.2
En este paciente, el hallazgo de un
aumento difuso de la glándula tiroides y la elevada vascularización en la
ecografía tiroidea sugieren tirotoxicosis inducida por amiodarona tipo 1. Esto
resalta la importancia de la evaluación tiroidea en pacientes tratados con
amiodarona, ya que la sobrecarga de yodo puede desencadenar un estado de
hiperfunción tiroidea en individuos predispuestos, lo cual tiene efectos
directos en el sistema cardiovascular.3
Además, la tirotoxicosis, incluso en sus
formas leves, aumenta la sensibilidad del miocardio a las catecolaminas y
altera la función eléctrica, lo que favorece la aparición de arritmias
malignas, en general, supraventriculares; sin embargo, las arritmias
ventriculares malignas, potencialmente mortales, rara vez, se relacionan con
esta entidad y suelen sobrevenir en pacientes con cardiopatía intrínseca, como
nuestro caso.4,5
Según diversos artículos consultados, el tratamiento de la crisis tirotóxica debe ser integral y escalonado. En este paciente, se utilizó un enfoque multidisciplinario que incluyó:
• Control de la actividad adrenérgica: se administró
esmolol en perfusión continua que, luego, se sustituyó por propranolol. Se
demostró que los betabloqueantes no selectivos mejoran la estabilidad
hemodinámica y reducen la respuesta arrítmica.2,6
• Bloqueo de la síntesis y liberación de hormonas tiroideas: se
indicó tiamazol y perclorato potásico para inhibir la organificación del yodo,
una estrategia recomendada en la tirotoxicosis inducida por amiodarona tipo 1.6,7
• Modulación de la respuesta inflamatoria: la dexametasona
contribuyó a la inhibición de la conversión periférica de T4 a T3 y a la reducción del estado hipermetabólico.7
• Manejo de la tormenta arrítmica: inicialmente, la procainamida fue
insuficiente para controlar las taquicardias ventriculares, lo que motivó la
administración de simpaticolíticos (dexmedetomidina y posteriormente clonidina)
como estrategia de estabilización.6
Todo esto permitió mejorar la estabilidad hemodinámica y facilitar la progresiva normalización de los niveles de T3.
Si la tirotoxicosis fuese resistente, podría considerarse la ablación con yodo radiactivo o incluso la tiroidectomía.2,6 Sin embargo, los pacientes con insuficiencia cardíaca grave deben ser evaluados cuidadosamente debido a los riesgos quirúrgicos.
Con respecto
al tratamiento de la insuficiencia cardíaca de este paciente, los siguientes
pasos fueron la optimización del manejo farmacológico y la evaluación para un
posible trasplante cardíaco. La disfunción valvular persistente y las
taquicardias ventriculares recurrentes, pese a los esfuerzos terapéuticos hacen
que el trasplante cardíaco sea una opción a largo plazo para mejorar su
supervivencia y calidad de vida.
Esto resalta la importancia de una estrategia terapéutica multidisciplinaria que involucre a especialidades, como Endocrinología, Cardiología y Cuidados Intensivos, para optimizar el manejo de estos pacientes.
Conclusiones
La crisis
tirotóxica inducida por amiodarona es un cuadro de alta complejidad,
especialmente en pacientes con cardiopatía estructural avanzada y
predisposición a arritmias ventriculares malignas. Este caso subraya la
necesidad de un diagnóstico precoz y un abordaje terapéutico multidisciplinario
para estabilizar al paciente y evitar desenlaces adversos.
La identificación temprana de la tirotoxicosis en pacientes que reciben tratamiento prolongado con amiodarona es fundamental para prevenir complicaciones potencialmente mortales.
Bibliografía
1.
Waqar Z,
Avula S, Shah J, Ali SS. Cardiovascular events in patients with thyroid storm.
J Endocr Soc 2021; 5(6): 1-8. https://doi.org/10.1210/jendso/bvab040
2.
Schubert
L, Bricaire L, Groussin L. Amiodarone-induced thyrotoxicosis. Ann Endocrinol
(Paris) 2021; 82(3-4): 163-166. https://doi.org/10.1016/j.ando.2020.04.009
3.
Shang W,
Ma QB. Malignant arrhythmias as the unmasked manifestation of thyroid storm.
Int J Gen Med 2020; 13: 693-698. https://doi.org/10.2147/IJGM.S265833
4.
Anjo D,
Maia J, Carvalho AC, Castro H. Thyroid storm and arrhythmic storm: a
potentially fatal combination. Am J Emerg Med 2013; 31(9): 1418.e3-5. https://doi.org/10.1016/j.ajem.2013.04.026
5.
Hamilton
D, Nandkeolyar S, Lan H, Desai P. Amiodarone: a comprehensive guide for
clinicians. Am
J Cardiovasc Drugs 2020; 20(6): 549-558. https://doi.org/10.1007/s40256-020-00401-5
6.
Correa
Guerrero J, Corrales Santander H, Yepes Caro J, Bello Simanca JD, Rodríguez Arrieta L, Castellanos Pinedo A, et al.
Tormenta tiroidea: abordaje diagnóstico y
terapéutico. Acta Colomb Cuid
Intensivo 2024; 34(4): 245-254. https://doi.org/10.1016/j.acci.2024.10.010
7.
Bartalena
L, Bogazzi F, Martino E. Management of amiodarone-induced thyrotoxicosis. Ther
Adv Endocrinol Metab 2012; 3(2): 47-58. https://doi.org/10.1177/2042018812437555